

Em mesas-redondas com representantes da Agência Nacional de Saúde Suplementar (ANS), Ana Cristina Martins, da Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec), Aline Silva, e da Secretaria de Atenção à Saúde do Ministério da Saúde, Eduardo Gomes de Souza, a diretora da Sociedade Brasileira de Oncologia Clínica (SBOC), Dra. Cinthya Sternberg, defendeu que tanto a ANS como a Conitec divulguem claramente os critérios utilizados para incorporar ou não cada medicamento oncológico ao rol de cobertura dos planos de saúde e à rede pública, respectivamente.
Novamente, a diretora colocou a SBOC à disposição para participar da avaliação técnica respaldada em evidências científicas para a decisão de passar a oferecer ou não determinado tratamento aos pacientes com câncer. De acordo com a Dra. Cinthya Sternberg, a SBOC quer participar não apenas de consultas públicas, mas contribuir desde o início para essas avaliações técnicas. “Entendemos que o processo mais correto é haver uma participação constante e direta da sociedade médica, sem intermediários”, frisou.
O debate ocorreu no dia 26 de abril, durante o VIII Fórum Nacional de Políticas de Saúde em Oncologia, promovido pelo Instituto Oncoguia em São Paulo. A diretora executiva da SBOC citou uma iniciativa da European Society for Medical Oncology (ESMO) como exemplo de medida que pode aperfeiçoar o processo. Trata-se da escala de benefício clínico. “À medida que são publicados novos estudos ou maturados dados de estudos que ainda não tinham sido aprofundados quando do registro de determinado medicamento, a recomendação da ESMO sobre aquela terapia pode ser reavaliada”, explica a Dra. Cinthya. “Permite uma tomada de decisão muito mais fluida, orgânica e próxima da realidade, utilizando, inclusive, quando possível, dados de real world e de pós-comercialização da droga.”
Transparência
A representante da SBOC frisou que a instituição vem intensificando o diálogo com os órgãos governamentais e que um dos principais pleitos é que sejam divulgados os critérios seguidos pela ANS e pela Conitec em suas decisões. “Muitas vezes, causa estranheza um parecer contrário à incorporação supostamente baseado em falta de evidências quando os oncologistas clínicos têm todos os dados que comprovam o mérito científico daquele medicamento”, pontua. “Se a decisão é econômica, precisamos saber disso e entender exatamente qual o critério adotado.”
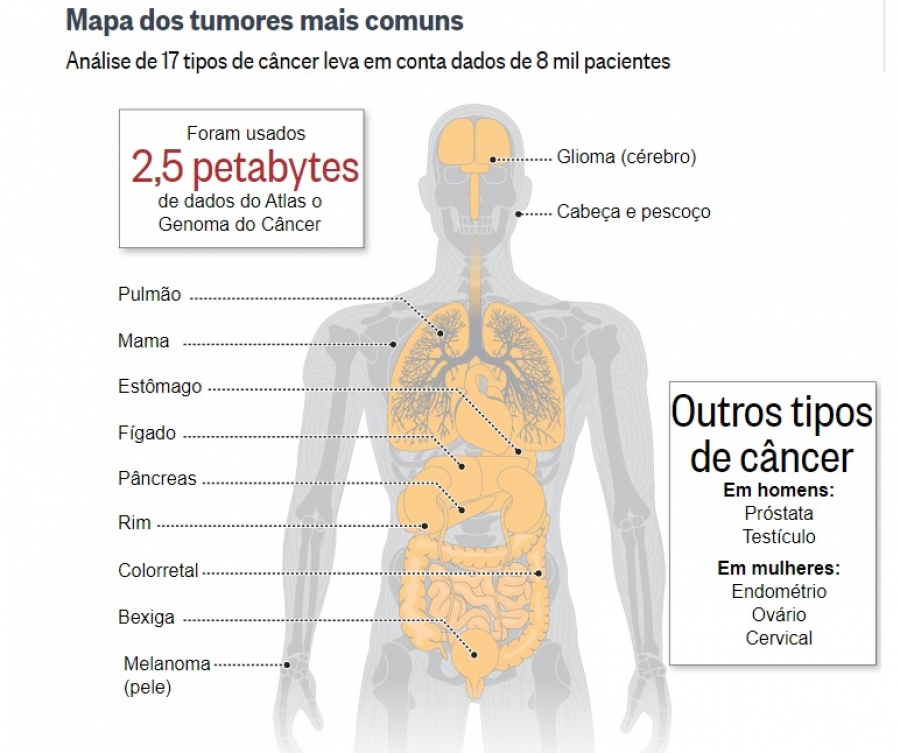
Conforme explicou a Dra. Cinthya Sternberg, o entendimento da SBOC sobre os tratamentos para os tipos de câncer mais frequentes na população brasileira estão nas diretrizes da Sociedade, publicadas no site. “Nesses guias de conduta está escrito o que os oncologistas clínicos consideram que deve ser oferecido a todos os pacientes, seja na saúde pública ou suplementar”, destaca. “São elencados somente medicamentos registrados pela Anvisa [Agência Nacional de Vigilância Sanitária]; não há nada off label ou sem registro.”
O diretor científico do Instituto Oncoguia e membro da SBOC, Dr. Rafael Kaliks, criticou o fato de haver duas agências do governo [ANS e Conitec] avaliando repetidamente se cada medicamento oncológico deve ou não ser oferecido para a população. “Uma vez que a Anvisa já concedeu o registro com base nos dados de eficácia e segurança e a sociedade médica recomenda a utilização da droga, é um absurdo que essas outras agências venham a discutir outra vez o mérito científico”, afirma. “A ANS não pode chegar a uma conclusão e a Conitec à outra”, continua o Dr. Rafael. “Depois de constatada a necessidade e a pertinência de um medicamento oncológico por um comitê competente, aí a questão de ‘como’ oferecer poderia ser considerada pela fonte pagadora: a pública ou a privada. Até porque a negociação com os fabricantes estaria baseada no número de pacientes que utilizariam aquele tratamento, o que pode mudar com a aprovação de uma nova indicação, por exemplo.” Contudo, atualmente, o oncologista clínico lembrou que a precificação é feita pela Câmara de Regulação do Mercado de Medicamentos (CMED), logo após o registro pela Anvisa, sem oportunidade de se estabelecer preços conforme cada situação de oferta e demanda. “Teríamos que redesenhar todo o sistema. Mas, por que não? Precisamos buscar uma saída para a escala de valores estratosféricos dos tratamentos e para os pacientes que estão sem acesso”, salienta.



















































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































Endereço
Avenida Paulista, 2073, Edifício Horsa II – Conjunto Nacional Conj. 1003, São Paulo/SP, 01311-300
Telefone
+55 (11) 3192-9284